Aerosolbildung in technischen Prozessen kann über spontane Phasenübergänge in übersättigten Gas- Dampf-Gemischen erfolgen. Die Schlüsselgröße ist hierbei der Sättigungsgrad S, der definiert ist als das Verhältnis der Summe der Partialdrücke aller kondensierbaren Komponenten, pD, bezogen auf den Sättigungsdampfdruck bei der aktuellen Temperatur und Zusammensetzung der Gasphase, pDS. Der Sättigungsdampfdruck entspricht dem Gemischtaupunkt bzw. dem Dampfdruck, wenn nur eine kondensierbare Komponente vorliegt:
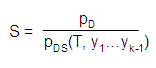
Übersättigungszustände (S > 1) können durch verschiedene Prozesse erzeugt werden, beispielsweise:
Mischungsvorgänge
chemische Reaktionen in der Gasphase
schnelles Entspannen von Gasen
simultane Wärme- und Stofftransportprozesse.
Durch simultane Wärme- und Stofftransportprozesse werden Übersättigungszustände in Gas-Flüssigkeitskontaktapparaten maßgeblich verursacht. Beispielsweise kann die Verdampfung von heißem Wasser in einen trockenen, kalten Inertgasstrom dazu genutzt werden, um gezielt ein Aerosol zu erzeugen.
Auf der anderen Seite kann Aerosolbildung auch unerwünscht sein, wie es bei der Absorption starker Säuren wie HCl, HBr oder H2SO4 in wässriger Lösung der Fall ist. Die Erzeugung von Übersättigungszuständen wird dadurch begünstigt, dass diese Säuren mit Wasser ein Azeotrop mit stark ausgeprägtem Dampfdruckminimum bilden. Wird beispielsweise eine heißes Rauchgas, das Spuren dieser Säuren enthält, gequencht, so können Tropfen gebildet werden, die oft eine erhebliche Schadstofffracht tragen und auf Grund ihrer Größe im Bereich um 1 µm (Minimum zwischen Diffusions- und Trägheitsabscheidung) schwierig abzuscheiden sind. Des Weiteren kann die Verschleppung der Tropfen in nachfolgende Prozessstufen dort betriebstechnische Probleme verursachen.
In Abb. 1 sind die Wärme- und Stoffaustauschvorgänge in einer Kolonne skizziert. Die Gasphase tritt mit einer Temperatur von 200°C in den Quench ein und wird mit der zirkulierenden Waschflüssigkeit, die Kühlgrenztemperatur (46°C) besitzt, in Kontakt gebracht. Als Laufkoordinate zur Beschreibung des Problems kann die Länge der Kolonne, z, oder auch die Phasengrenzfläche A bzw. der NTU Wert, der einer entdimensionierten Phasengrenzfläche entspricht, gewählt werden.
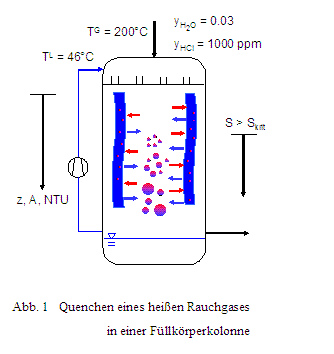 |
Die Gasphase steht in einem intensiven Kontakt mit der Flüssigphase, das über die Füllkörperschüttung bzw. die Packung läuft. Durch diesen intensiven Kontakt erfahren Gas- und Flüssigphase eine simultane Zustandsänderung, die sich in der Abkühlung der Gasphase, der Absorption der Säurekomponente in der Waschflüssigkeit und der Verdampfung von Wasser äußert. |
Durch diese Zustandsänderung kann der Taupunkt der Gasphase überschritten werden, so dass sich die Gasphase übersättigt. Sobald der Sättigungsgrad größer als der kritische Sättigungsgrad ist, entstehen, eingeleitet durch homogene oder heterogene Keimbildung, Tropfen, die im weiteren Verlauf der Kolonne anwachsen. Durch die Aerosolbildung müssen die Zustandsänderungen von drei Phasen mit einem konkurrierenden Stoffaustausch zwischen Gas- und Flüssigphase sowie Gasphase und Aerosol simultan berechnet werden.
| |
Zur Berechnung der Aerosolbildung in Gas-Flüssigkeitskontaktapparaten wurde am Institut in Kooperation mit dem Konrad-Zuse-Zentrum für Informationstechnik, Berlin, das Simulationsprogramm AerCoDe entwickelt, dessen Aufbau in Abb. 2 schematisch dargestellt ist. In AerCoDe werden die Gas- und Flüssigkeitsströmung eindimensional als Propfenströmungen betrachtet und es konnte experimentell bestätigt werden, dass diese Betrachtung trotz der ablaufenden komplexen fluiddynamischen Vorgänge eine gute Beschreibung technischer Apparate liefert. |
Die Modellierung in AerCoDe beruht nun auf der Betrachtung von 4 unterschiedlichen Bilanzräumen für die Flüssigphase, die Phasengrenze, die Gasphase und die Tropfenphase. Für alle Bilanzräume wurden eindimensionale, differentielle Massen- und Energiebilanzen entlang der Laufkoordinate aufgestellt. Sie sind gekoppelt durch den Wärme- und Stoffaustausch zwischen den Bilanzräumen. Die Bilanzgleichungen und Modellansätze ergeben ein differential-algebraisches Gleichungssystem, das numerisch an verschiedenen Stützstellen im Apparat gelöst wird.
| |
In Abb. 3 ist ein Prozesspfad für die Absorption von HCl in einem Quench mit zirkulierender Waschflüssigkeit dargestellt. Das Rauchgas tritt mit einer Temperatur von 200°C in den Quench ein und wird mit einer Flüssigkeit von 46°C (Kühlgrenze) gekühlt. Die Säurebeladung im Eintritt beträgt 1000 ppm. |
An der Ordinate ist die Summe der Partialdrücke von Wasser und HCl als Funktion der Zusammensetzung der Gasphase, d.h. die Taulinien für Temperaturen zwischen 45°C und 50°C aufgetragen. Zusätzlich sind in diesem Gleichgewichtsdiagramm p-y Punkte des Prozesspfads eingezeichnet. Der Prozess startet bei hohen HCl Molanteilen und niedrigen Partialdrücken der kondensierbaren Komponenten und verläuft durch die Verdampfung von Wasser und die Absorption von HCl zu geringeren Molanteilen und höheren Partialdrücken. Um festzustellen, wann ein Taupunkt überschritten wird, sind die Punkte des Prozesspfads mit den entsprechenden Temperaturen beschriftet. Die Gasphase ist übersättigt, sobald der Taupunkt bei der entsprechenden Temperatur überschritten ist. In Abb. 3 kann man sehen, dass dies ab einer Temperatur von 47°C der Fall ist, allerdings sind die erreichten Übersättigungen nicht sonderlich groß, da die Taulinie nicht massiv überschritten wird. Bei diesen geringen Übersättigungen findet keine homogene Keimbildung statt, die Tropfenbildung erfolgt an im System vorhandenen Fremdkeimen.
Berücksichtigt man bei den Rechnungen die heterogene Keimbildung, so zeigt sich, dass sich die Übersättigung durch das Wachstum der gebildeten Tropfen abbaut. In welchem Ausmaß dies geschieht, hängt maßgeblich damit zusammen, wie groß die Zahl der Fremdkeime im Prozess ist. In Abb. 4 ist der Sättigungsgrad für den Fall ohne Aerosolbildung sowie für typische Fremdkeimkonzentrationen zwischen 105 und 107 Keimen/cm³ als Funktion des NTU Wertes dargestellt.
Man kann deutlich erkennen, dass die Übersättigung umso schneller abgebaut wird, je größer die Zahl der Fremdkeime im System ist. Das liegt daran, dass das Tropfenkollektiv mit der größeren Anzahlkonzentration die größere Stoffaustauschfläche besitzt.
Der Durchmesser, auf den die gebildeten Tropfen anwachsen, ist näherungsweise umgekehrt proportional zu ihrer Anzahlkonzentration. Abb. 5 zeigt die Tropfendurchmesser für die gewählten Fremdkeimkonzentrationen. Am Kolonnenende werden bei diesem Beispiel Tropfendurchmesser zwischen 300 und 900 nm erreicht.
Neben Prozessen mit heterogener Keimbildung, können auch Prozesse, in denen homogene Keimbildung auftritt, mit AerCoDe berechnet werden. Dabei muss die Anzahlkonzentration der Tropfen aus der Keimbildungsrate J, z.B. nach der klassischen Theorie homogener Keimbildung berechnet werden.
Der Einsatz von AerCoDe ist nicht beschränkt auf Prozesse in Kolonnen bzw. Gas-Flüssigkeits-Kontaktapparaten. Solange ein entsprechendes Modell für den Wärme- und Stoffübergang vorhanden ist, können alle Prozesse, in denen Übersättigungszustände durch simultane Wärme- und Stofftransportprozesse erzeugt werden, berechnet werden.
Für heterogene Keimbildung ergibt sich eine sehr gute Übereinstimmung zwischen Theorie und Praxis [1,2], für homogene Keimbildung ist der Validierungsprozess Gegenstand aktueller Forschungsarbeiten.
Literatur:
[1] R. Ehrig, O. Ofenloch, K. Schaber, P. Deuflhard:
Modelling and simulation of aerosol formation by heterogeneous nucleation in gas - liquid contact devices.
Chem. Eng. Science 57 (2002) 1151-1163.
[2] K. Schaber, J. Körber, J., O. Ofenloch, R. Ehrig, P. Deuflhard:
Aerosol formation in gas-liquid contact devices - nucleation, growth and particle dynamics.
Chem. Eng. Science 57 (2002) 4345-4356.
[3] A. Wix, K. Schaber, O. Ofenloch, R. Ehrig, P. Deuflhard:
Simulation of aerosol formation in gas-liquid contact devices.
Eingereicht zur Publikation in Chem. Eng. Communication, 2006.


